Thermodynamique
La thermodynamique est une branche récente de la physique, développée au 19e, siècle qui s’intéresse aux conversions d’énergie en lien avec la température.
Gaz parfaits
L’état gazeux est dispersé et désordonnée.
À l’échelle microscopique, les entités qui le composent sont éloignées les unes des autres et ont un mouvement aléatoire incessant.
Pour le décrire parfaitement, il faudrait connaître la masse, la position et la vitesse de chacune des entités...
À l’échelle macroscopique, on utilise 3 grandeurs intensives (ne dépendant pas du volume) qui moyennent de manière complémentaire
le chaos microscopique :
- la masse volumique $\rho$
qui dit combien les entités sont serrées en moyenne
- la pression $P$ qui renseigne sur la force moyenne par unité de surface provoquée due aux chocs incessants des entités
- la température $T$ qui correspond à l'énergie cinétique moyenne des entités (traduisant
l'agitation des entité)
Ces trois grandeurs sont liées entre elles
dans la loi des gaz parfaits.
Mais généralement, on lui préfère la forme faisant intervenir la quantité de matière et le volume
à la place de la masse volumique.
Loi des gaz parfaits :
- $P$ : pression (en $\color{#FFF056}\pu{Pa}$)
- $V$ : volume (en $\color{#FFF056}\pu{m3}$)
- $n$ : quantité de matière (en $\color{#FFF056}\pu{mol}$)
- $T$ : température (en $\color{#FFF056}\pu{K}$)
- $R$ : constante des gaz parfaits
$R= 8,314$ $\color{#FFF056}\pu{Pa*m3*K-1*mol-1}$
Rq :
La pression est aussi une énergie par unité de volume.
$\Rightarrow \pu{Pa} = $ $\pu{J*m-3}$
Et donc $R$ s'exprime en $\pu{J*K-1*mol-1}$
Un gaz est dit parfait si la taille des entités est négligeable devant la distance qui les sépare et
si les interactions entre elles sont négligeables.
Limites du modèle
Dans le modèle GP, on néglige le volume
des entités et on néglige leurs interactions.
Dans quelles gammes de pression et de température ces approximations peuvent-elles s'avérer fausses ?
- À haute pression, les entités deviennent si serrées que l'effet de leur volume devient non négligeable.
- À basse température, l'énergie cinétique des entités devient du même ordre de grandeurs que leur énergie de liaison.
Moralité, le modèle du gaz parfait marche pour une pression pas trop grande ($P<\pu{10 bar}=\pu{1 MPa}$).
Et pour une température très supérieure à la température d'ébullition du gaz ($T\gg T_{vap}$).
Comme l’air se liquéfie vers -190°C à pression atmosphérique ($P_{atm}\approx \pu{1 bar}$), l’ai peut être considéré comme une GP aux conditions
ordinaires de température et de pression.
Énergie interne
L’énergie interne $U$ d’un système résulte
des énergie cinétique (liée à l’agitation)
et potentielle (liée aux interactions)
de l’ensemble des entités qui le composent.
La variation d’énergie interne
d’un système incompressible (solide ou liquide)
est proportionnelle à sa variation de température.
Le coefficient de proprortionnalité est
la capacité thermique $C$ du système.
- $\Delta U$ en J
- $\Delta T$ en K
- $C$ en $\pu{J*K-1}$
Naturellement, plus le système contient d’entités,
plus son énergie interne sera grande.
Pour caractériser un matériau
indépendamment de sa masse, on utilise
la capacité thermique massique $c$.
- $\Delta U$ en J
- $\Delta T$ en K
- $m$ en kg
- $c$ en $\pu{J*K-1*kg-1}$
Plus la capacité thermique d’un corps est grande,
plus il est facile / difficile de modifier sa température.
| Matériau | Capacité thermique massique (J·kg⁻¹·K⁻¹) |
|---|---|
| Eau liquide | 4 185 |
| Glace (à 0°C) | 2 100 |
| Huile (végétale) | 2 000 |
| Aluminium | 897 |
| Brique | 840 |
| Acier | 450 – 500 |
Premier principe de la thermodynamique
L’énergie totale d’un système est la somme de son énergie mécanique et de son énergie interne :
L’énergie d’un système fermé (qui n’échange pas
de matière avec l’extérieur) peut varier par
échange d’énergie avec l’extérieur.
Cet échange peut prendre deux formes :
- travail $W$ de forces non conservatives
(comme le travail des forces de pression) - transfert thermique $Q$
Pemier principe de la thermodynamique
Pour un système isolé :
Et si le système est immobile :
Par convention, les transferts d’énergie sont comptés positivement lorsqu’ils entrent dans le système
et négativement quand ils en sortent.
Prenons l’exemple du système
{résistance chauffante d’une bouilloire électrique} :
- Le travail électrique $W$
est compté positivement - Le transfert thermique $Q$ avec l'eau
est compté négativement
Si on considère le système
{eau de la bouilloire},
il n’y a plus de travail,
mais deux transferts thermiques :
- Le transfert thermique $Q_r$ avec
la résistance compté positivement - Le transfert thermique $Q_e$ avec
l'extérieur compté négativement
Rq :
Rien n'empêche que tous les transferts
soient positifs ou tous négatifs.
Exemple ?
Modes de transfert thermique
Il y a trois modes de transfert thermique :
- la conduction
- la convection
- le rayonnement
Un transfert thermique par conduction
a lieu de proche en proche.
Il n'y a pas déplacement macroscopique de matière.
L'agitation microscopique des entités
est communiquée de l'une à l'autre.
Aérogel de silice, polystyrène expansé, laine de roche, laine de verre, liège expansé, ouate de cellulose…
Qu'ont en commun les meilleurs isolants thermiques ?
Un transfert thermique par convection
ne peut avoir lieu que dans un fluide.
Il correspond à un mouvement macroscopique de matière : le fluide est animé d'un mouvement interne.
Comment expliquer ce mouvement d'ensemble ?

Qu’est-ce que c’est ?
Discuter le matériau, la forme et l’orientation.
Petite énigme
Pourquoi un glaçon fond-il moins vite dans
de l'eau salée que dans de l'eau douce ?
Le transfert thermique par rayonnement est
le seul à pouvoir se faire dans le vide.
Il correspond à l'émission ou l'absorption
d'ondes électromagnétiques.
Comment marche une couverture de survie ?

Comment expliquer ce qu’on voit dans cette vidéo ?
Flux thermique
Le flux thermique est la puissance qui traverse une surface au cours d’un transfert thermique.
C'est donc l'énergie thermique $Q$ par unité de temps.
- $Q$ en J
- $\Delta t$ en s
- $\Phi$ en W
Comme pour le transfert thermique $Q$ et le travail $W$, le flux thermique $\Phi$ est compté positivement s’il entre dans le système et négativement s’il en sort.
Résistance thermique
Le flux thermique par conduction et/ou convection
à travers un milieu séparé par deux surfaces
aux températures $T_f$ et $T_c >T_f$ s’effectue
de la surface froide vers la surface chaude.
Pour traduire l’aptitude du milieu à résister
au passage du flux thermique, on définit
la résistance thermique $R_{th}$ comme :
- $\Delta T$ en $\pu{K}$
- $\Phi$ en $\pu{W}$
- $R_{th}$ en $\pu{K*W-1}$
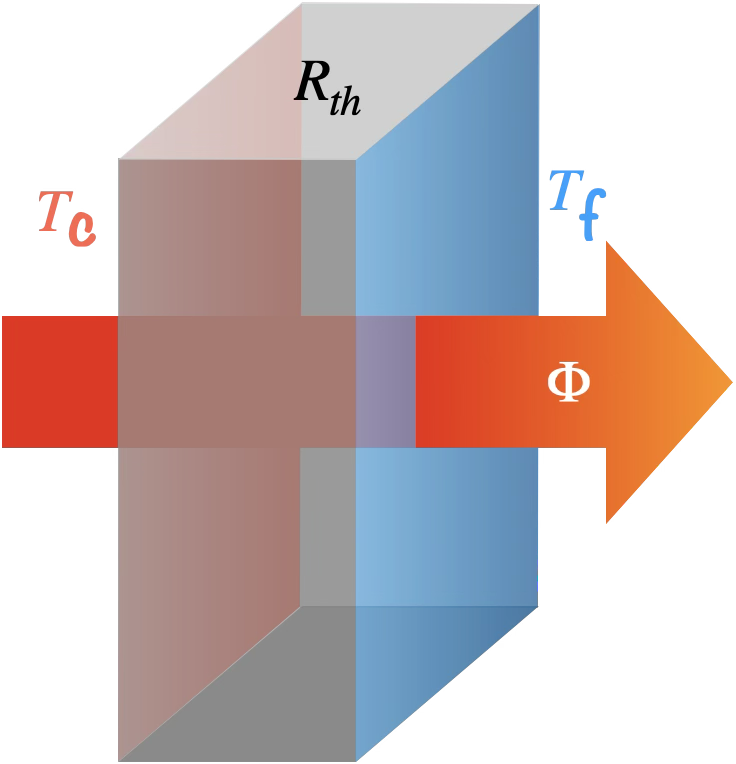
Analogie électrique :
- $R_{th}$ $\longleftrightarrow$ $R$
- $\Phi$ $\longleftrightarrow$ $I$
- $\Delta T$ $\longleftrightarrow$ $U$
Pour une même différence de température,
plus la résistance thermique du milieu est grande
et plus le flux thermique est faible.
Si les parois du matériau sont planes (mur par exemple), la résistance thermique de conduction peut s’exprimer en fonction de la surface $S$ des parois, de l’épaisseur $e$ entre les deux parois et de la conductivité thermique $\lambda$ caractérisant le matériau :
$\lambda$ s'exprime en $\pu{W*m-1*K-1}$.
Rq : cette formule sera toujours donnée.
Dans le cas d’un contact avec un fluide, le flux thermique est dit conducto-convectif.
On peut construire une résistance thermique $R_\text{th cv}$
à l'aide d'un coefficient de transfert thermique $h$ :
$$R_\text{th cv}=\frac{1}{hS}$$
unité de $h$ : $\pu{W*m-2*K-1}$
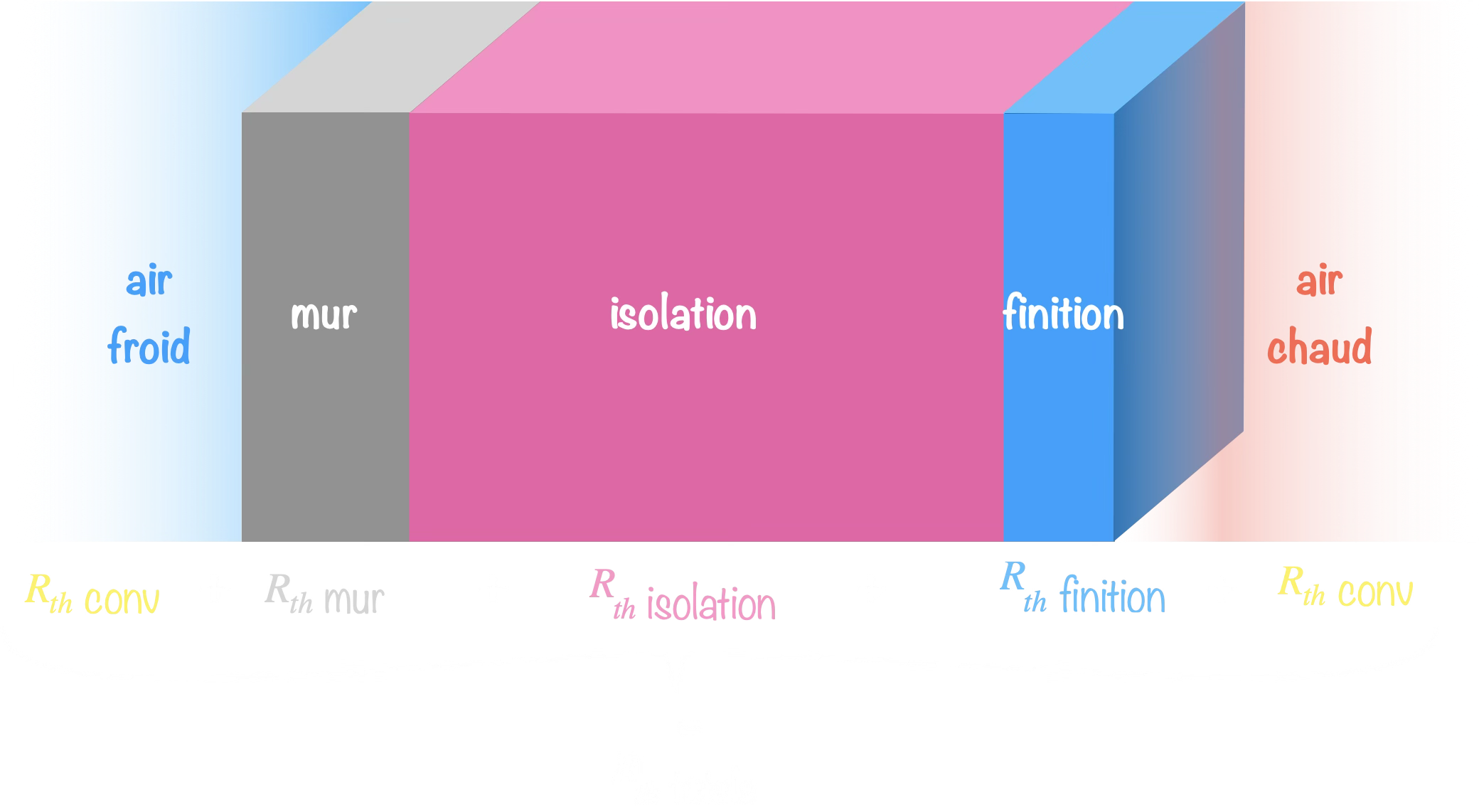
Des résistances en série s’additionnent.
Évolution temporelle de la température d’un système
La loi phénoménologique de Newton (aussi appelée loi du refroidissement de Newton) modélise le transfert thermique entre un système et le milieu extérieur
par convection et conduction.
Elle énonce que le flux thermique antre un système et le milieu extérieur est proportionnel à la différence de température entre ce système et le milieu extérieur.
$$\Phi = h S \left(T_\mathrm{ext}-T\right)$$
$T$ est la température du système.
Rq : cette formule (ou une ressemblante)
sera toujours fournie.
- $S$ (surface de la paroi) en $\pu{m2}$
- $h$ (coefficient d'échange conducto-convectif)
en$\pu{W*m-2*K-1}$
Si la température d’un système peut être considérée comme constante (il suffit qu’il soit suffisamment
gros par exemple), on parle de thermostat.
On considère très souvent le milieu extérieur
comme un thermostat $\Rightarrow T_\mathrm{ext}\approx \mathrm{cte}$.
Modélisons l’évolution de la température $T(t)$ d’un système incompressible en contact avec un thermostat.
Pour cela, réalisons un bilan d’énergie du système
entre les instants $t$ et $t+\Delta t$ :
- On suppose que le système est immobile.
- On suppose que le système ne reçoit aucun travail.
- Le système échange une énergie thermique $Q$ avec le thermostat (l'extérieur).
D'après le 1er principe de la thermodynamique :
Pendant la durée $\Delta t$, l’énergie thermique échangée s’exprime en fonction du flux thermique comme :
Et comme le système est incompressible,
on peut écrire :
$\Delta T$ est la variation de température du système
entre les instants $t$ et $t+\Delta t$.
Enfin, d’après la loi phénoménologique de Newton :
On a donc :
$$ \begin{aligned} \Delta U = mc\Delta T &= Q\\ &={\color{#FFF056}\Phi}\Delta t\\ &={\color{#FFF056}hS\left(T_\mathrm{ext}-T(t)\right)}\Delta t \end{aligned} $$
On obtient :
Et en réarrangeant :
Faisons tendre le laps de temps $\Delta t$ vers 0 :
On obtient alors :
D’où :
Et finalement :
On reconnaît une équation différentielle du 1er ordre
à coefficients constants avec second membre :
Où $ \tau = \frac{mc}{hS}$ est le temps caractéristique de l'évolution.
Solution :
où $T_0=T(0)$ est la température initiale.
On obtient logiquement que :
- Si $T_0 < T_\mathrm{ext} $, $T(t)$ est croissante,
le système se réchauffe. - Si $T_0 > T_\mathrm{ext}$, $T(t)$ est décroissante,
le système se refroidit.
Et dans tous les cas, lorsque $t\to\infty$
(en pratique pour $t>5\tau$), le système est
à la température du thermostat $T_\mathrm{ext}$.
On appelle cela l'équilibre thermique.
Bilan thermique du système
{Terre, atmosphère}
Le système reçoit de l'énergie par
transfert thermique radiatif du Soleil.
Le système perd de l'énergie par
transfert thermique radiatif vers l'espace.
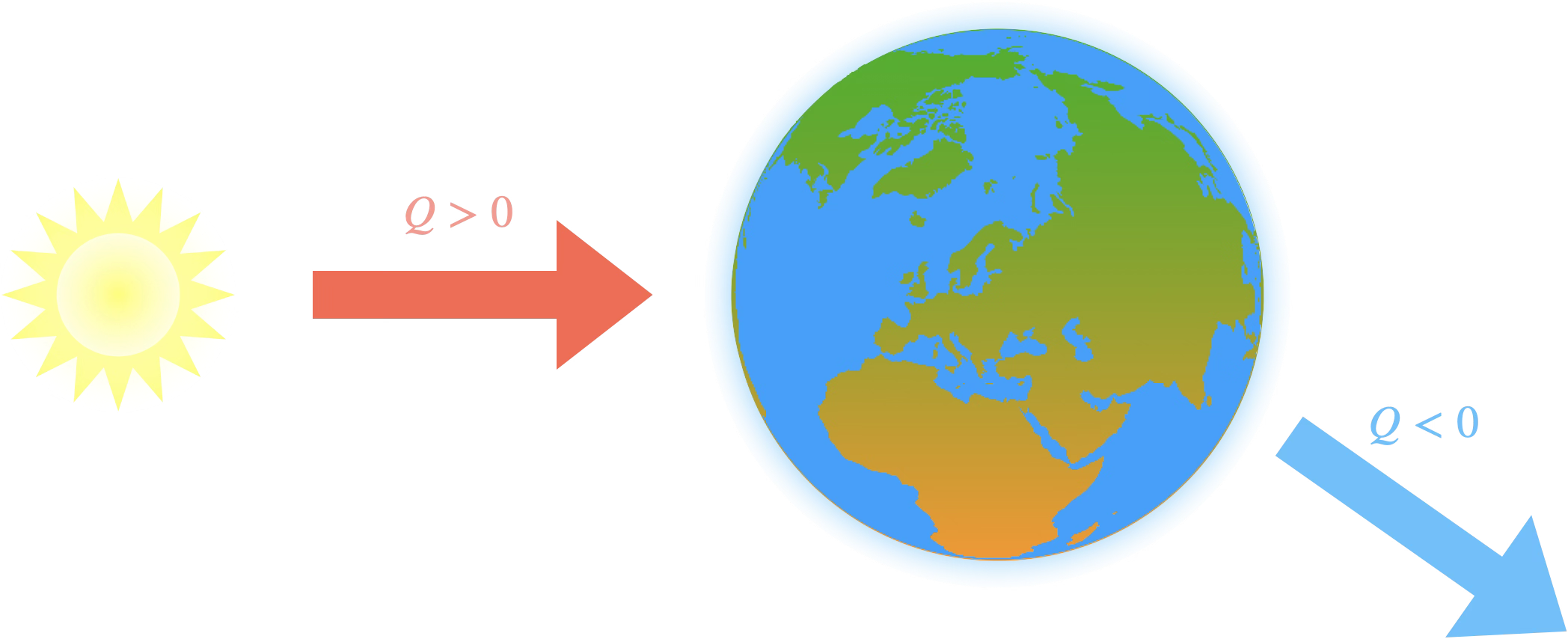
Il y a donc un flux entrant (positif) $\Phi_{\mathrm{entrant}}$
et un flux sortant (négatif) $\Phi_{\mathrm{sortant}}$.
Et plutôt que le flux total $\Phi$, on se concentre
sur le flux surfacique $\varphi$ (flux par $\pu{m^2}$).
Une partie du flux entrant est rediffusé directement vers l’espace (par les nuages et le sol suivant sa nature).
entre le flux diffusé $\varphi_D$ et le flux entrant :
Grâce à sa couverture nuageuse, l’albédo de
la Terre est relativement élevé ($\approx$ 30%)
quand celui de la Lune vaut 7% seulement…
La carte suivante, réalisée à partir des données du projet CERES de la NASA, montre le rayonnement solaire directement réfléchi $\varphi_D$.
On a là une partie du flux sortant $\varphi_\mathrm{sortant}$.
Mais il en manque beaucoup pour équilibrer
le flux solaire $\varphi_\mathrm{entrant} = \pu{340,4 W*m-2}$...
D'où vient le reste ?
Du rayonnement de la Terre !
Tout corps à température $T$ émet un rayonnement électromagnétique dont le flux thermique
surfacique vérifie la loi de Stefan-Boltzman :
- $\varphi$ en $\pu{W*m-2}$
- $T$ en $\pu{K}$
- $\sigma =\pu{5,67E-8}$ $\pu{W*m^2*K^{-4}}$
$\sigma$ est la constante de Stefan-Boltzmann.
On voit que le Soleil rayonne dans le visible alors que
la Terre émet dans l’infrarouge, autour de 10 μm.
Or une partie des gaz atmosphériques ($\ce{CO2}$, $\ce{H2O}$, $\ce{CH4}$, etc.) absorbe les infrarouges
(cf. spectroscopie infrarouge).
Et ce rayonnement absorbé est diffusé dans toutes
les directions, donc pour moitié vers la surface.
Il est alors plus difficile pour la Terre
d’évacuer sa chaleur, c’est l’effet de serre.
Conséquence : la surface se réchauffe jusqu'à ce que
le flux sortant $\varphi_\mathrm{sortant}$ redevienne suffisant
pour équilibrer le flux entrant.
L’augmentation dans l’atmosphère de la concentration des gaz à effet de serre déplace à nouveau l’équilibre.
Le déséquilibre $\varphi_\mathrm{entrant} >\varphi_\mathrm{sortant}$ entraîne une $\nearrow$
de la température de surface qui va à son tour
$\nearrow$ $\varphi_\mathrm{sortant}$ jusqu'à retour à l'équilibre.
Le déséquilibre par rapport à l’année de référence préindustrielle 1750 est appelé forçage radiatif
et vaut aujourd’hui plus de $\pu{3,0 W*m-2}$.
Tableau de bord interactif
du réchauffement climatique.
On peut réaliser un bilan radiatif simplifié
avec un modèle monocouche de l’atmosphère qui absorberait une proportion $\alpha$ du rayonnement infrarouge $\varphi_E$ émis par la Terre.
On appellera dans la suite $\varphi_S$ le flux solaire entrant.
D’après le schéma :
Et à l'équilibre, on doit avoir :
Cela permet d’exprimer $\varphi_E$ en fonction de $\varphi_S$ :
Et comme $\varphi_E=\sigma T^4$, on en déduit :
Influence de $\alpha$ :
Actuellement, la valeur de $\alpha$ est aux alentours de 80%.
Influence de $A$ :